Форма выпуска и состав
Лейкостим выпускают в форме раствора для подкожного и внутривенного введения:
- 150 мкг: во флаконах по 1 мл, по 5 флаконов в картонной пачке;
- 300 мкг: во флаконах по 1 или 1,6 мл, по 5 флаконов в картонной пачке либо по 1 или 5 флаконов в контурных пластиковых упаковках, по 1 упаковке в картонной пачке;
- В стеклянных шприцах с иглами по 0,5 или 1 мл, по 1 или 5 шприцов в картонной пачке;
- 600 мкг: в шприцах по 0,8 мл, по 1 или 5 шприцов в контурных ячейковых упаковках, по 1 упаковке в картонной пачке).
В состав 1 мл входит активное вещество: филграстим – 150, 300 или 600 мкг.
Аналоги
Совпадения по коду АТХ 4-го уровня:
Нейпоген
Нейпомакс
Граноцит
Тимоген
Тактивин
Граноген, Грасальва, Лейцита, Нейпоген, Миеластра, Нейпомакс, Нейростим, Филергим.
Показания к применению
- Нейтропения (в т.ч. у пациентов, получающих цитостатические лекарственные средства при лечении немиелоидных злокачественных новообразований);
- Стойкая нейтропения у больных с развернутой стадией ВИЧ-инфекции (при абсолютном числе нейтрофилов 1000 клеток/мкл и меньше);
- Нейтропения (наследственная, идиопатическая или периодическая при числе нейтрофилов ниже или равном 500 клеток/мкл) и тяжелые или рецидивирующие инфекции (в анамнезе) в течение последних 12 месяцев.
Также Лейкостим применяют для сокращения продолжительности периода нейтропении и ее клинических последствий у больных, которые готовятся к трансплантации костного мозга и для мобилизации периферических стволовых клеток (в т.ч. после проведения миелосупрессивной терапии).
Отзывы о Лейкостиме
Отзывов пациентов, принимавших этот препарат мало. Например, имеются отзывы о применении этого препарата при циклической нейтропении и иммунной нейтропении у детей. При этих тяжелых заболеваниях эффект от препарата был непродолжительным.
Чаще встречаются результаты клинического применения Лейкостима у взрослых и детей с нейтропенией, ассоциированной с химиотерапией новообразований. Так, детям препарат назначался в дозе 5 мкг/кг в сутки, хорошо переносился. Есть результаты клинических исследований, целью которых было сравнение переносимости и эффективности Лейкостима и Нейпогена. Были сделаны выводы: сроки устранения нейтропении при применении этих препаратов не различаются, и они имеют идентичные показатели переносимости и эффективности.
Способ применения и дозировка
Лейкостим вводят подкожно (предпочтительно) или внутривенно. При необходимости внутривенного введения препарата, требуемое количество Лейкостима с 5% раствором декстрозы следует ввести из шприца во флакон или пластиковый контейнер, затем провести в течение 30 минут инфузию. Препарат нельзя разводить 0,9% раствором натрия хлорида. Также не следует разводить филграстим до конечной концентрации меньше 2 мкг/мл (0,2 млн МЕ/мл).
Применение препарата не рекомендовано меньше чем за 24 часа до начала и раньше, чем через 24 часа после окончания курса химиотерапии.
Дозы и способ введения определяются конкретной клинической ситуацией.
При нейтропении Лейкостим следует вводить 1 раз в день внутривенно или подкожно по 5 мкг на 1 кг массы тела больного после курса цитотоксической химиотерапии.
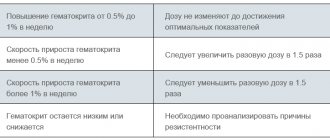
У получающих цитотоксическую химиотерапию больных преходящее увеличение числа нейтрофилов обычно наблюдается через 1-2 дня после начала терапии. Для оценки эффективности проводимого лечения желательно ежедневно подсчитывать количество нейтрофилов в периферической крови. Терапию рекомендуется проводить до тех пор, пока число нейтрофилов не достигнет нормальных значений. Лейкостим можно отменить после достижения абсолютного числа нейтрофилов, превышающего 2,0×109/л. При необходимости продолжительность лечебного курса может составить до 12 дней.
После проведения миелоаблативной химиотерапии с последующей пересадкой костного мозга, Лейкостим следует вводить внутривенно или подкожно из расчета 10 мкг на 1 кг массы тела. Первую дозу нужно вводить не раньше, чем через 24 часа после цитотоксической химиотерапии, при трансплантации костного мозга – не позже, чем через 24 часа после инфузии костного мозга. Суточную дозу Лейкостима корректируют после того, как пройдет момент максимального снижения числа нейтрофилов. В случаях, когда содержание нейтрофилов в периферической крови выше 1,0х109/л на протяжении трех дней подряд, дозу Лейкостима снижают в 2 раза (до 5 мкг на 1кг массы тела). Затем, если в течение трех дней подряд абсолютное число нейтрофилов превышает 1,0х109/л, Лейкостим отменяют. При уменьшении абсолютного числа нейтрофилов в процессе терапии ниже 1,0х109/л, дозу вновь увеличивают до 10 мкг на 1 кг массы тела.
При применении Лейкостима с целью мобилизации кроветворных стволовых клеток рекомендовано подкожное введение в суточной дозе 5 мкг (у пациентов после миелосупрессивной химиотерапии) или 10 мкг на 1 кг массы больного (в отсутствие химиотерапии) на протяжении 5-7 последовательных дней (количество введений определяется результативностью сепарации и скоростью нарастания количества лейкоцитов в периферической крови). За день до проведения первой сепарации (на четвертый день введения Лейкостима) и в течение следующих дней до дня последней сепарации следует оценивать количество нейтрофилов и лейкоцитов в периферической крови пациента. Цитаферез проводят в случаях увеличения числа лейкоцитов до 5х109/л периферической крови, начиная с пятого дня введения Лейкостима. После каждой сепарации нужно подсчитывать число СD34+ клеток и ядросодержащих клеток в предназначенном для криоконсервации образце. Введение Лейкостима прекращают при достижении количества криоконсервированных СD34+ клеток, достаточного для проведения трансплантации (не меньше 2×106 на 1 кг массы пациента).
Безопасность и эффективность применения Лейкостима у здоровых доноров младше 16 и старше 60 лет не исследовалась.
При лечении тяжелой хронической нейтропении (ТХН) Лейкостим нужно вводить подкожно ежедневно. Применение препарата прекращают после того, как число нейтрофилов будет стабильно превышать 1,5х109/л (при врожденной нейтропении – в дозе 12 мкг на 1 кг массы больного в день подкожно за одно или несколько введений; при периодической или идиопатической нейтропении – 5 мкг на 1 кг массы в день). Для поддержания этого уровня нейтрофилов определяют минимальную эффективную дозу. Для этого требуется ежедневное продолжительное введение препарата. В зависимости от реакции больного через 7-14 дней терапии начальную дозу можно увеличить или уменьшить в 2 раза. В дальнейшем каждые 7-14 дней нужно проводить коррекцию дозы для поддержания числа нейтрофилов в пределах 1,5-10х109/л.
При лечении ассоциированной с ВИЧ-инфекцией нейтропении Лейкостим вводят подкожно однократно в начальной дозе 1-4 мкг на 1 кг массы тела в день до нормализации числа нейтрофилов (больше 2х109/л). Как правило, нормализация числа нейтрофилов происходит через 2 дня. При неэффективности терапии проводят эскалацию дозы до 5 мкг на 1 кг массы в день однократно подкожно. После достижения терапевтического эффекта переходят на поддерживающую терапию – 2-3 раза в неделю по 1-4 мкг на 1 кг массы в день. В дальнейшем возможна индивидуальная коррекция дозы.
Фармакологические свойства
Фармакодинамика
Активное вещество Лейкостима – филграстим, является высокоочищенным негликозилированным белком, состоящим из 175 аминокислот. Он вырабатывается штаммом Escherichia coli, в геном которой введен ген Г-КСФ (гранулоцитарного колониестимулирующего фактора человека) с использованием методов генной инженерии. Человеческий Г-КСФ является гликопротеином, регулирующим образование функционально активных нейтрофилов и их выход из костного мозга в кровь.
В результате применения Лейкостима на протяжении 24 часов после введения в периферической крови значительно возрастает число нейтрофилов с небольшим увеличением количества моноцитов. При ТХН (тяжелой хронической нейтропении) филграстим может приводить к незначительному увеличению числа циркулирующих базофилов и эозинофилов. У некоторых из этих больных еще до начала лечения может выявляться базофилия или эозинофилия.
Филграстим дозозависимо увеличивает количество нейтрофилов с нормальной/повышенной фагоцитарной и хемотаксической активностью. После окончания терапии число нейтрофилов в периферической крови уменьшается на 50% за 1–2 дня, к нормальному уровню показатель возвращается в течение последующих 1–7 дней.
Применение Лейкостима позволяет значительно уменьшить частоту, продолжительность и тяжесть нейтропении и фебрильной нейтропении, при этом снижается необходимость и длительность стационарного лечения у больных, получающих химиотерапию цитостатиками или миелоаблативное лечение с последующей трансплантацией костного мозга.
Пациентам, получающим Лейкостим и цитотоксическую химиотерапию, требуются меньшие дозы антибиотиков в сравнении с больными, получающими цитотоксическую химиотерапию без филграстима.
На фоне применения препарата значительно уменьшается длительность фебрильной нейтропении, потребность в проведении антибиотикотерапии и госпитализации после индукционной химиотерапии у пациентов с острым миелолейкозом. При этом филграстим на частоту лихорадки и инфекционных осложнений влияния не оказывает.
Применение Лейкостима как самостоятельно, так и после окончания химиотерапии способствует мобилизации выхода гемопоэтических стволовых клеток в периферический кровоток. Аллогенная или аутологичная трансплантация ПСКК (периферических стволовых клеток крови) проводится после терапии большими дозами цитостатиков, либо вместо/в дополнение к трансплантации костного мозга. Трансплантация ПСКК также может быть назначена после миелосупрессивного цитотоксического лечения. Применение ПСКК, мобилизованных с помощью филграстима, позволяет ускорить восстановление кроветворения, уменьшить опасность геморрагических осложнений и потребность в переливании тромбоцитарной массы после миелоаблативной или миелосупрессивной терапии.
Профиль безопасности/эффективности Лейкостима у взрослых и детей, получающих цитотоксическую химиотерапию, не отличается.
У детей и взрослых на фоне ТХН (тяжелой врожденной, периодической, идиопатической нейтропении) филграстим стабильно увеличивает количество нейтрофилов в периферической крови, уменьшает частоту инфекционных осложнений.
При назначении Лейкостима пациентам с ВИЧ-инфекцией появляется возможность поддерживать нормальный уровень нейтрофилов и соблюдать рекомендованные дозы антиретровирусной и/или иной миелосупрессивной терапии. Признаки увеличения репликации ВИЧ на фоне терапии филграстимом не отмечаются.
Как и прочие гемопоэтические факторы роста, Г-КСФ на человеческие эндотелиальные клетки оказывает стимулирующее действие.
Канцерогенные свойства филграстима не изучены. Филграстим мутации в геноме бактерий, независимо от наличия ферментной системы, необходимой для метаболизма препарата, не вызывает.
Установлено, что определенные злокачественные клетки на своей поверхности имеют рецепторы к Г-КСФ. Нельзя исключить того, что филграстим может служить фактором роста для различного типа опухолей.
При проведении исследований на крысах обоего пола при применении филграстима в дозах до 500 мкг/кг какое-либо влияние на фертильность и протекание беременности обнаружено не было.
В исследованиях на кроликах и крысах филграстим тератогенным эффектом не обладал. У кроликов отмечалась повышенная частота выкидышей, при этом аномалии развития плода выявлены не были.
Фармакокинетика
Филграстим после подкожного введения быстро всасывается и своей максимальной концентрации в сыворотке крови достигает за 2–8 часов. Период полувыведения после внутривенного или подкожного введения обычно находится в диапазоне 2–4 часа. Клиренс и период полувыведения определяются дозой и количеством нейтрофилов. Можно предположить о преобладании линейного характера клиренса и фармакокинетических процессов.
Абсолютная биологическая доступность после подкожного введения 375 и 750 мкг составляет 62% и 72% соответственно. Концентрация филграстима после прекращения его введения снижается до значений эндогенных величин за 24 часа.
У пациентов с онкологическими заболеваниями и здоровых добровольцев перед проведением химиотерапии при многократном введении филграстима было выявлено снижение его плазменной концентрации. Увеличение клиренса вещества в данном случае является дозозависимым, предположительно степень этого увеличения зависит от степени нейтрофилии у реципиентов. Это согласуется с информацией об увеличении нейтрофилзависимого клиренса при возрастании пула нейтрофилов. У пациентов, которые получают филграстим после проведения химиотерапии, плазменная концентрация вещества остается на одном уровне вплоть до момента начала восстановления гемопоэза.
При внутривенном и подкожном введении филграстима отмечается положительная линейная зависимость между дозой и концентрацией в сыворотке крови. После подкожного введения терапевтических доз концентрация филграстима превышает 10 нг/мл на протяжении 8–16 часов. Объем распределения составляет 150 мл/кг.
При длительном назначении филграстима (курсом до 28 дней) после аутологичной трансплантации костного мозга кумуляция и изменение периода полувыведения не отмечаются.
Вне зависимости от способа введения выведение филграстима протекает по правилам кинетики первого порядка. Период полувыведения составляет 3,5 часа, клиренс – 0,6 мл/мин/кг.
Фармакокинетика филграстима у детей после проведения химиотерапии сходна с таковой у взрослых, которые получают такие же дозы препарата с учетом массы тела. Это позволяет сделать вывод о независимости фармакокинетических процессов Лейкостима от возраста.
При терминальной стадии почечной недостаточности отмечается тенденция к увеличению системной экспозиции филграстима в сравнении со здоровыми добровольцами и пациентами с клиренсом креатинина в диапазоне 30–60 мл/мин.
Побочные действия
Применение Лейкостима может сопровождаться болями в мышцах и костях, а также болезненностью в месте инъекции.
У 7,5% больных были отмечены умеренные или слабые костно-мышечные боли, которые лекарственной коррекции не требовали либо купировались нестероидными противовоспалительными препаратами. Сильных болей во время терапии отмечено не было.
В редких случаях в месте введения препарата могут развиваться реакции гиперчувствительности замедленного типа, сопровождающиеся появлением отека и эритемы (при их развитии применение Лейкостима следует прекратить).
В отдельных случаях при применении препарата наблюдались гепатомегалия, утомляемость, головная боль, диарея, расстройства мочеиспускания (главным образом, умеренная или слабая дизурия). Были отдельные сообщения о преходящем понижении артериального давления (лечение не требовалось). Также возможно развитие обратимого, дозозависимого и обычно слабого или умеренного повышения концентраций щелочной фосфатазы, лактатдегидрогеназы, сывороточной мочевой кислоты и гамма-глутамилтрансферазы, понижение числа тромбоцитов в периферической крови.
Редко может возникать кожная сыпь, тромбоз сосудов, васкулит, а также увеличение селезенки у пациентов с исходно не увеличенной селезенкой. Возможно появление инфильтратов в легких с развитием респираторного дистресс-синдрома взрослых. Такие явления чаще возникали после применения схем химиотерапии, включающих блеомицин, их связь с приемом Лейкостима не установлена. Очень редко после применения препарата наблюдались случаи развития гематурии и протеинурии.
Исключительно редко при применении препарата обострялся ревматоидный артрит, при длительном применении может возникать разрыв селезенки, анемия, тромбоцитопения, а также кожный васкулит у больных с тяжелой хронической нейтропенией.
Особые указания
Лечение Лейкостимом должно проводиться только под контролем врача-онколога или гематолога, имеющего опыт применения подобных лекарственных препаратов. Перед его назначением следует исключить такие причины развития преходящей нейтропении, как вирусные инфекции.
Особое внимание необходимо уделять диагностике тяжелых хронических нейтропений, чтобы дифференцировать их от других гематологических заболеваний, таких как миелолейкоз, миелодисплазия и апластическая анемия.
При хроническом миелолейкозе и миелодиспластическом синдроме безопасность и эффективность применения филграстима не установлены. Больным с данными заболеваниями и с предопухолевыми поражениями миелоидного ростка кроветворения назначение Лейкостима не рекомендовано, т.к. клетки некоторых опухолей могут нести рецептор к гранулоцитарному колониестимулирующему фактору. По этой причине особое внимание следует уделять дифференциальной диагностике между бластным кризом хронического миелолейкоза и острым миелолейкозом.
Во время терапии необходимо постоянно контролировать размеры селезенки (путем пальпации живота). Согласно данным исследований, при снижении дозы Лейкостима увеличение селезенки останавливается или, как минимум, замедляется.
У небольшого числа (около 3%) пациентов с Синдромом Костманна, получавших филграстим, наблюдались лейкоз и миелодиспластический синдром – естественные осложнения этого заболевания, связь которых с применением препарата не установлена. В случае развития этих осложнений Лейкостим следует отменить.
В редких случаях (менее 5%) у пациентов, проходящих курс лечения филграстимом, отмечался гиперлейкоцитоз (увеличение числа лейкоцитов выше 100х109/л), поэтому нужно регулярно определять количество лейкоцитов. При их увеличении более 50×109/л Лейкостим нужно отменить. Если препарат применяется для мобилизации кроветворных стволовых клеток, его нужно отменить при повышении числа лейкоцитов более 70×109/л.
Примерно у 12% больных с исходно нормальной цитогенетикой при повторном исследовании выявлялись аномалии, включая моносомию 7. Если у пациентов с тяжелой врожденной нейтропенией обнаруживаются цитогенетические нарушения, следует взвесить преимущества и возможные риски продолжения терапии. Каждые 12 месяцев необходимо проводить цитогенетические и морфологические исследования костного мозга.
Важно учитывать, что Лейкостим не предотвращает анемию и тромбоцитопению, которые часто являются следствием применения химиотерапевтических препаратов в высоких дозах. Поэтому во время лечения после химиотерапии следует регулярно определять количество тромбоцитов и эритроцитов, а также уровень гемоглобина.
Влияние на способность к управлению автотранспортом и сложными механизмами
Учитывая механизм фармакологического действия филграстима, его влияние на скорость психомоторных реакций и способность к концентрации внимания представляется крайне маловероятным.
Лекарственное взаимодействие
Нужно соблюдать интервал в 24 часа (до или после) при одновременном применении Лейкостима с миелосупрессивными препаратами.
Безопасность и эффективность введения филграстима в один день с цитотоксическими химиопрепаратами не установлена.
Фармацевтически Лейкостим не совместим с 0,9% раствором натрия хлорида.
При одновременном назначении с филграстимом 5-фторурацил может усиливать тяжесть нейтропении.
Применяя препарат с целью мобилизации кроветворных стволовых клеток после химиотерапии, нужно учитывать, что при назначении на протяжении длительного времени таких цитостатиков, как карбоплатин, кармустин (BCNU) и мелфалан, эффективность мобилизации может быть уменьшена.
Противопоказания
Абсолютные:
- Синдром Костманна (тяжелая врожденная нейтропения) с цитогенетическими нарушениями;
- Применение с целью увеличения доз цитотоксических химиопрепаратов, превышающих рекомендованные;
- Одновременное применение с цитотоксической химио- и лучевой терапией;
- Период лактации;
- Индивидуальная непереносимость компонентов препарата.
Относительные (Лейкостим назначается с осторожностью):
- Серповидно-клеточная анемия;
- Патология костной ткани (включая остеопороз);
- Вторичный острый миелолейкоз (связано с ограниченностью данных по безопасности/эффективности);
- Применение в сочетании с высокодозной химиотерапией;
- Беременность.
Оценка безопасности и эффективности не проводилась:
- Дети до 16 лет после миелосупрессивной или миелоаблативной терапии с последующей аутологичной трансфузией ПСКК;
- Новорожденные с тяжелой хронической нейтропенией.